ADC薬物開発におけるPK研究での抗MMAE/MMAFペイロード抗体の使用
ADC(抗体薬物複合体)薬物開発において、薬物動態(PK)研究は、抗体、リンカー、細胞毒性薬物を含むADCおよびその構成要素の体内での挙動を理解するために重要です。モノメチルオーリスタチンE(MMAE)またはモノメチルオーリスタチンF(MMAF)を細胞毒性ペイロードとして使用するADCに焦点を当てる場合、抗MMAE/MMAF抗体が重要な役割を果たすことがあります。
| Cat No. | Product Description | Fc | Products Information |
| GTU-Bios-Auristatin-Ab-01 | Anti-MMAE/MMAF monoclonal antibody | hFc/mFc | Details |
| GTU-Bios-Auristatin-Ab-02 | Anti-MMAE monoclonal antibody | hFc/mFc | Details |
用途
競争的免疫測定法(競争的ELISA)およびその他の免疫測定法,
抗体薬物複合体(ADC)のMMAEペイロードに対するPK & PDアッセイ
ハイライト
純度: ≥95% (SDS-PAGE)
高い親和性と特異性が検証済み
ADCの結合アッセイによる高感度が確認済み
GeneMediのGMP-Bios-Auristatin-Ab:MMAEおよびMMAFベースのADCに対する精密な結合
GeneMediのGTU-Bios-Auristatin-Ab-01-2は、MMAEまたはMMAFペイロードを組み込んだADCに対して強力な結合親和性を示し、標的薬物送達における多用途性を強調しています。これに対し、GTU-Bios-Auristatin-Ab-02-2は、MMAEベースのADCに対して専用の特異性を示し、最小限のオフターゲット効果で精密な標的化を実現します。さらに、いずれの抗体もDXDと結合したADCとは結合を示さず、GeneMediの最適化された治療結果を実現するために特別に設計された高選択性抗体の製造に対する取り組みを強調しています。
- 図1:コーティングPTM-1 MMAE
- 図2:コーティングPTM-1 MMAF
- 図3:コーティングPTM-1 DXD
- 図4:薬物動態(PK)研究
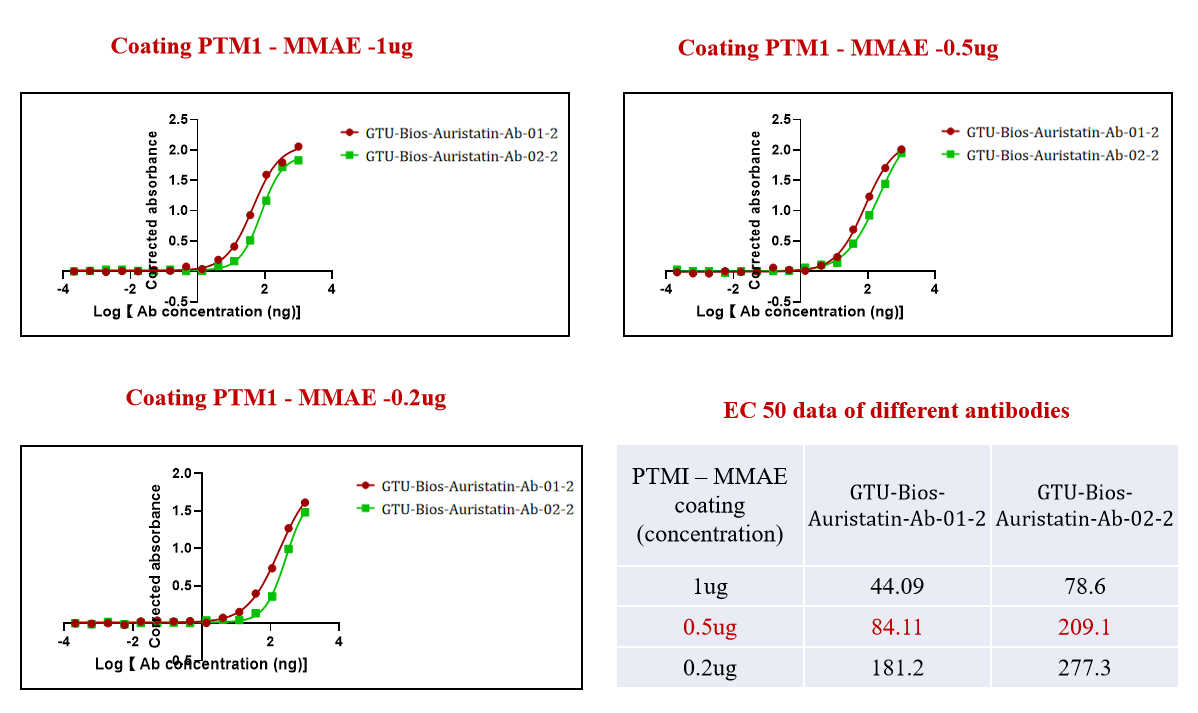
図1. GTU-Bios-Auristatin-Ab-01-2とGTU-Bios-Auristatin-Ab-02-2が ADC (PTM-1 MMAE)と積極的に結合しています。
図1は、GeneMediのGTU-Bios-Auristatin-Ab-01-2とGTU-Bios-Auristatin-Ab-02-2が ADC (PTM-1 MMAE)と積極的に結合する有効性を示しています。これはMMAEベースのADCと効果的に結合するためにカスタムメイドされた 高品質抗体を生産するGeneMediの取り組みを強調しています。
図に示されている強力な結合は、抗体-薬物複合体(ADC)分野におけるGeneMediの専門性を証明しており、これは標的薬物送達に 最適化された抗体の開発における重要な側面です。
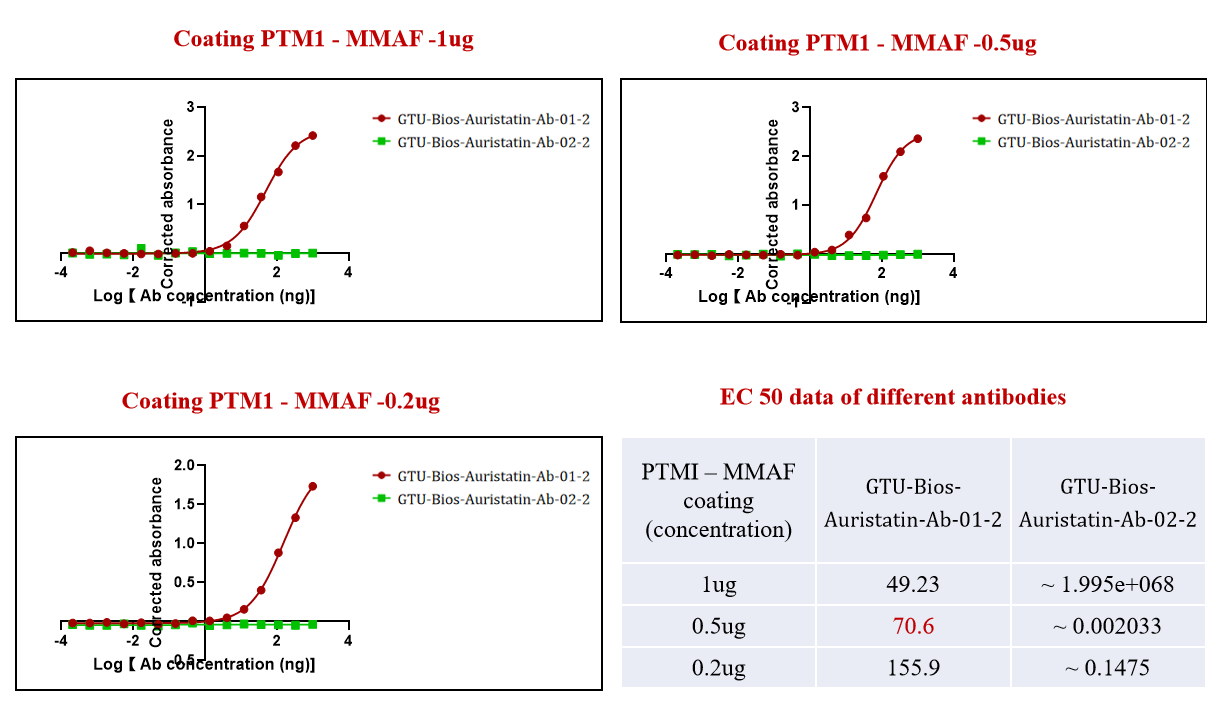
図2. GTU-Bios-Auristatin-Ab-01-2はADC (PTM-1 MMAF)と 積極的に結合しましたが、GTU-Bios-Auristatin-Ab-02-2はMMAFと結合していません。
図2はGTU-Bios-Auristatin-Ab-01-2がADC (PTM-1 MMAF)と成功裏に 結合する一方で、GTU-Bios-Auristatin-Ab-02-2は結合していないという点でGeneMediの抗体特異性を示しています。こうした 特異性はMMAEを含むADCの標的精度を保証し、治療効果を高めながら非標的効果を最小限に抑えるのに重要です。
GeneMediが異なる薬物ペイロードと選択的に結合する抗体をカスタムメイドする能力は、抗体エンジニアリングの 分野におけるその熟練度を示しており、研究者に対して精密医療応用に信頼できるツールを提供します。
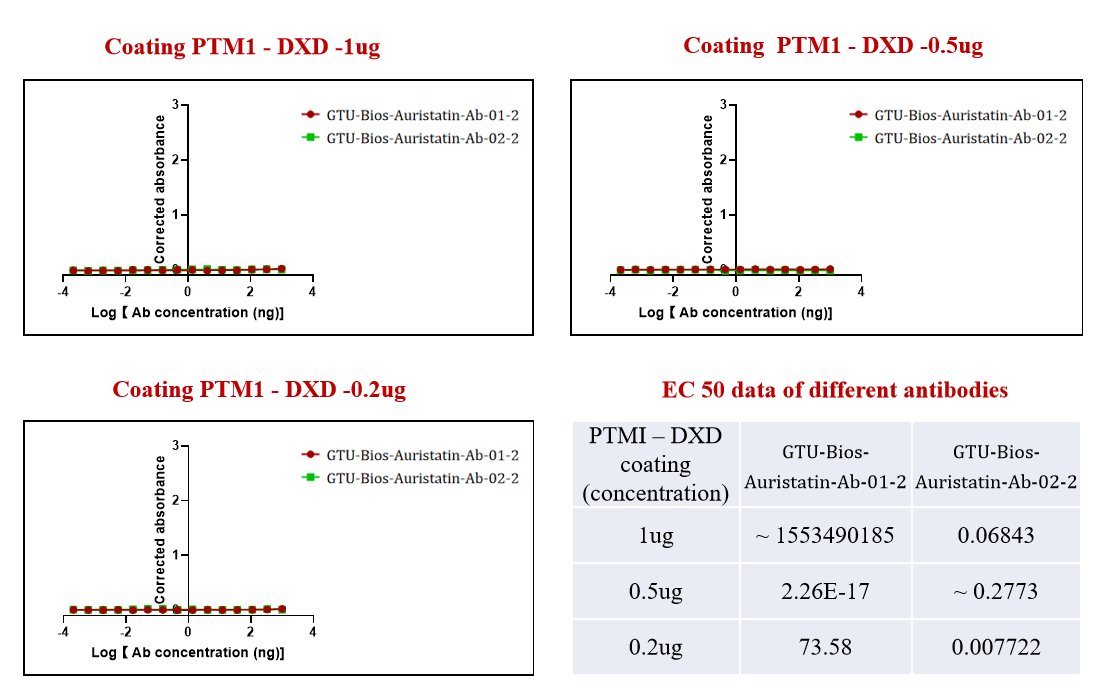
図3. GTU-Bios-Auristatin-Ab-01-2とGTU-Bios-Auristatin-Ab-02-2がDXDで 結合したADCと結合していません。
図3はGeneMediの抗体特異性の別の側面を示しており、 GTU-Bios-Auristatin-Ab-01-2とGTU-Bios-Auristatin-Ab-02-2がDXDで結合したADCと結合しないことを 示しています。このデータは、望ましくないペイロードとの干渉を最小限に抑える高選択性抗体を生産するための GeneMediの取り組みを強調しています。
交差反応がほとんどない抗体を提供することにより、GeneMediは研究者に対して癌治療のためのADCの設計および最適化に 精密なツールを提供し、最終的には生物医学研究および臨床応用の最前線を前進させています。
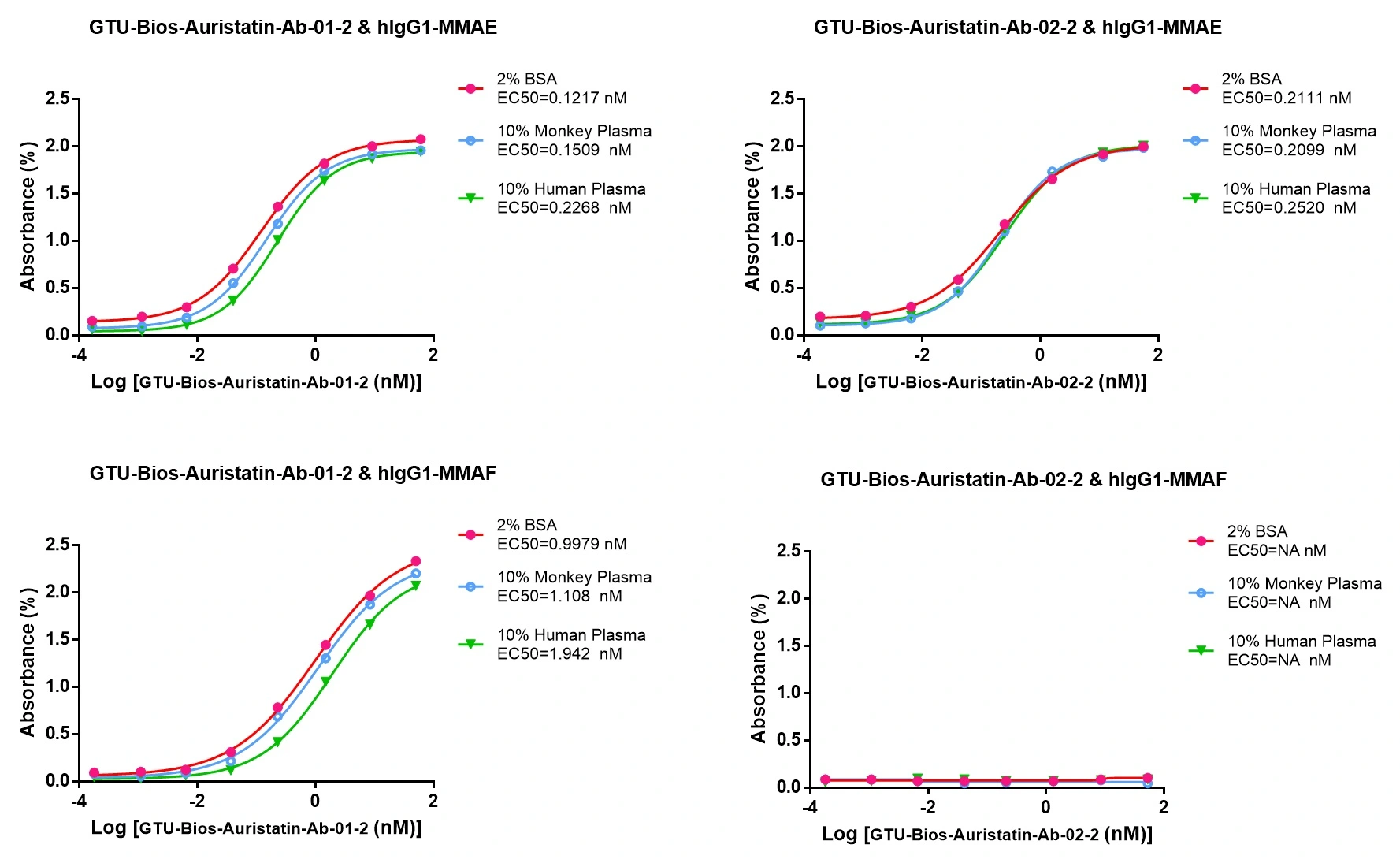
図4: GTU-Bios-Auristatin-Ab-01-2とGTU-Bios-Auristatin-Ab-02-2は ヒトおよびサルを対象とした薬物動態(PK)研究に使用できます
GTU-Bios-Auristatin-Ab-01-2はヒトおよびサルのPK研究において 最小限の影響を示し、無視できるレベルです。GTU-Bios-Auristatin-Ab-02-2はこれらのPK研究において GTU-Bios-Auristatin-Ab-01-2よりも影響が少ないです。GTU-Bios-Auristatin-Ab-01-2と GTU-Bios-Auristatin-Ab-02-2はヒトおよびサルのPK実験に適しています。
PK研究における抗MMAE/MMAF抗体の役割
-
検出と定量:
-
抗MMAE/MMAF抗体は、ADC投与後に放出されたり循環中に残存するMMAE/MMAFのレベルを特定して定量するために使用されます。これは、ADCの安定性および薬物放出速度を評価するために重要です。
-
-
ADCの完全性の評価:
-
これらの抗体を使用して循環中の遊離MMAE/MMAFを測定することで、ADCのリンカーの安定性を推測することができます。遊離薬物の濃度が高い場合、リンカーが安定していない可能性があり、細胞毒性薬物の早期放出につながる可能性があります。
-
-
安全性と有効性の相関:
-
MMAE/MMAFの薬物動態を理解することで、薬物濃度と治療効果および潜在的な毒性を関連付けることができます。抗MMAE/MMAF抗体は、さまざまな生物学的マトリックス中の薬物の正確な測定を提供することで、これを支援します。
-
-
免疫原性試験:
-
ADCは免疫反応を引き起こし、抗薬物抗体(ADA)の生成をもたらす可能性があり、それが薬物の有効性と安全性に影響を与える可能性があります。抗MMAE/MMAF抗体は、薬物自体とそれに対して形成されたADAを区別するために使用できます。
-
ADC薬物開発への応用
-
-
前臨床および臨床開発: 前臨床および臨床フェーズの両方で、抗MMAE/MMAF抗体は薬物の分布、分解、および排泄をモニターするためのアッセイに使用されます。この情報は、投与スケジュールの最適化および最小限の毒性で最大の治療効果を確保するために重要です。
-
規制コンプライアンス: これらの抗体を使用したPK研究から得られたデータは、薬物の体内での挙動に関する詳細な情報を提供することにより、規制要件を満たすのに役立ちます。これは承認プロセスにおいて重要です。
-
製剤の最適化: PK研究から得られた洞察は、ADCの製剤の最適化に役立ちます。例えば、MMAE/MMAFの早期放出が観察された場合、リンカー化学または抗体自体の変更を考慮して安定性を向上させることができます。
-
このように、PK研究における抗MMAE/MMAF抗体の使用は、MMAE/MMAFベースのADCの成功した開発に不可欠であり、早期の研究から臨床試験までの薬物開発の多くの側面を導くための重要なデータを提供します。






 Facebook
Facebook LinkedIn
LinkedIn Twitter
Twitter
