ADC薬物開発における薬物動態(PK)研究における抗ペイロード抗体
ADC(抗体薬物複合体)に対する抗ペイロード抗体は、フリーの細胞毒性薬物を中和し、副作用を減少させることで、安全性と有効性を向上させることを目的としています。これらの抗体は、精密な薬物送達を可能にし、治療プロファイルを改善し、薬物モニタリングを可能にします。これは、パーソナライズド治療戦略の可能性を秘めた、ターゲットがん治療の重要な進展を示しています。
ADC(抗体薬物複合体)に対する抗ペイロード抗体は、フリーの細胞毒性薬物を中和し、副作用を減少させることで、安全性と有効性を向上させることを目的としています。これらの抗体は、精密な薬物送達を可能にし、治療プロファイルを改善し、薬物モニタリングを可能にします。これは、パーソナライズド治療戦略の可能性を秘めた、ターゲットがん治療の重要な進展を示しています。
| Cat No. | Payload | Product Name | Fc | Technical Information | Products Information |
| GTU-Bios-Maytansinoids-Ab | DM1/DM4 | Anti-DM1/DM4 monoclonal antibody(mAb) | hFc/mFc | More | Details |
| GTU-Bios-Auristatin-Ab-01 | MMAE/MMAF | Anti-MMAE/MMAF monoclonal antibody(mAb) | hFc/mFc | More | Details |
| GTU-Bios-Auristatin-Ab-02 | MMAE (Specific) | Anti-MMAE (Specific) monoclonal antibody(mAb) | hFc/mFc | More | Details |
| GTU-Bios-DXd-Ab | DXd/Exatecan | Anti-DXd&Exatecan monoclonal antibody(mAb) | hFc/mFc | More | Details |
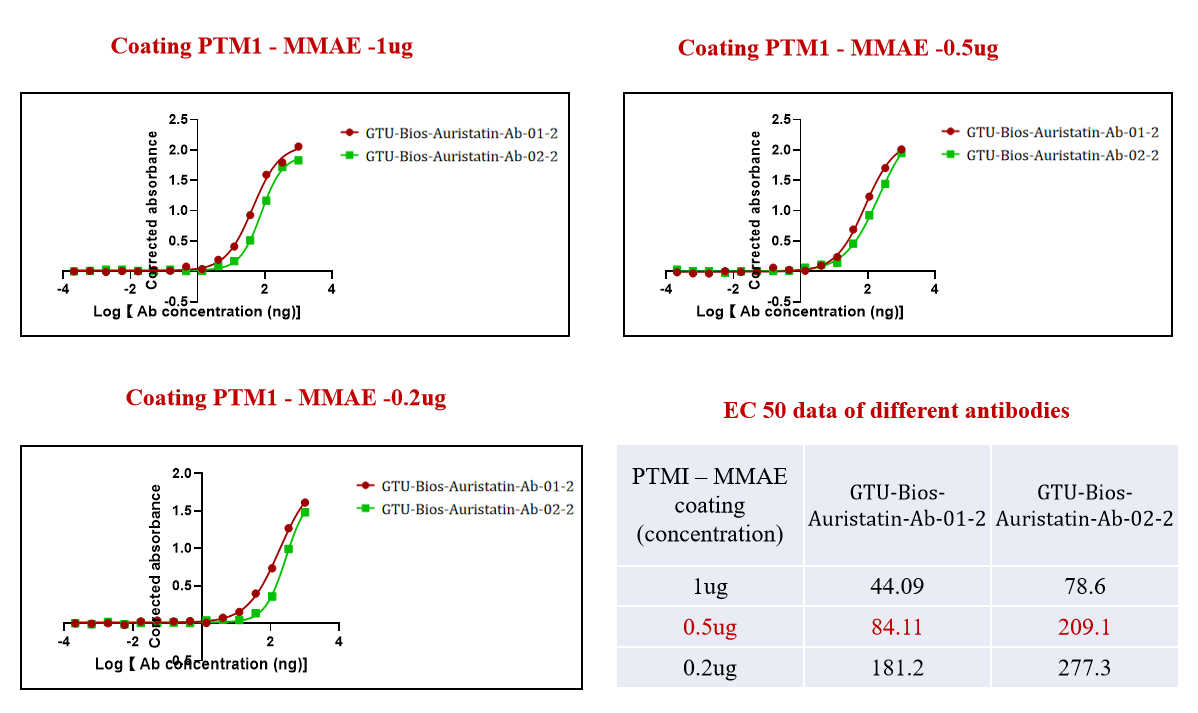
図1. GMP-Bios-MMAE-Ab-2およびGMP-Bios-MMAE-Ab-3はADC(PTM-1 MMAE)と積極的に結合しています。
図1は、GeneMediのGMP-Bios-MMAE-Ab-2およびGMP-Bios-MMAE-Ab-3がADC(PTM-1 MMAE)と積極的に結合している効果を示しています。これは、MMAEベースのADCと効果的に結合するために特化した高品質の抗体を製造するというGeneMediのコミットメントを示しています。
図に示された強固な結合は、ターゲット薬物送達の分野で重要な要素である抗体薬物複合体(ADC)の開発におけるGeneMediの専門知識を強調しています。
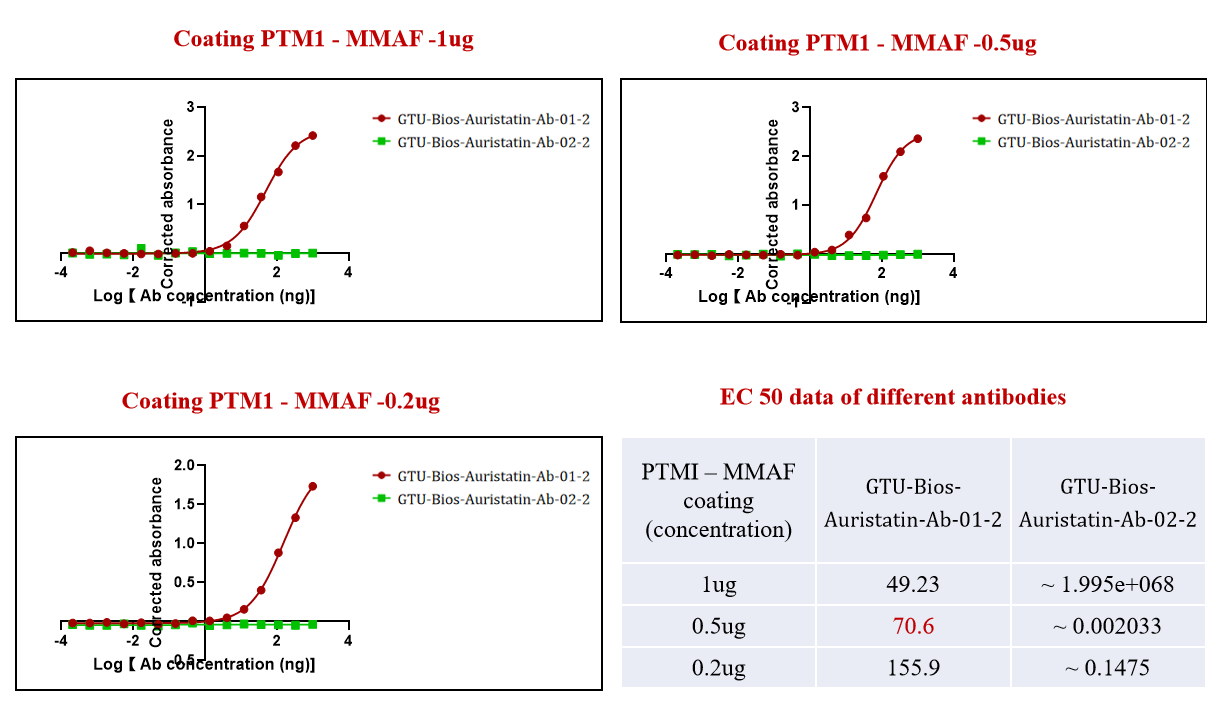
図2. GMP-Bios-MMAE-Ab-2はADC(PTM-1 MMAF)と積極的に結合していますが、GMP-Bios-MMAE-Ab-3はMMAFと結合していません。
図2では、GMP-Bios-MMAE-Ab-2がADC(PTM-1 MMAF)と成功裏に結合している一方で、GMP-Bios-MMAE-Ab-3は結合していないことが示されています。この特異性は、MMAEを含むADCの正確なターゲティングを保証し、副作用を最小限に抑える上で重要です。
GeneMediが特定の薬物ペイロードに選択的に結合するように抗体をカスタマイズする能力は、精密医学のアプリケーションに信頼性の高いツールを提供する彼らの抗体工学の熟練度を示しています。
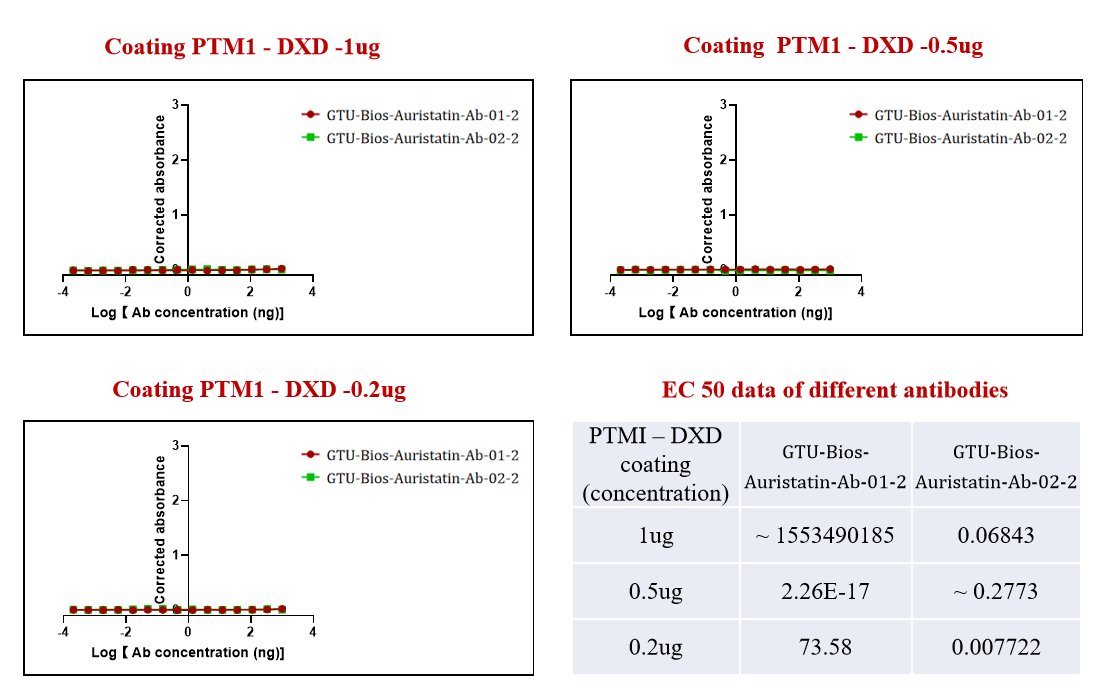
図3. GMP-Bios-MMAE-Ab-2およびGMP-Bios-MMAE-Ab-3はDXDで結合したADCと結合していません。
図3は、GeneMediの抗体の特異性の別の側面を示しており、GMP-Bios-MMAE-Ab-2およびGMP-Bios-MMAE-Ab-3のいずれも、DXDで結合したADCとは結合していないことが明らかにしています。このデータは、不要なペイロードとの干渉を最小限に抑えるために高い選択性を持つ抗体を製造するというGeneMediの取り組みを強調しています。
交差反応性が最小限である抗体を提供することにより、GeneMediは研究者に対して、ターゲットがん治療のためのADCの設計と最適化に正確なツールを提供し、バイオメディカル研究と臨床応用の最前線を前進させます。
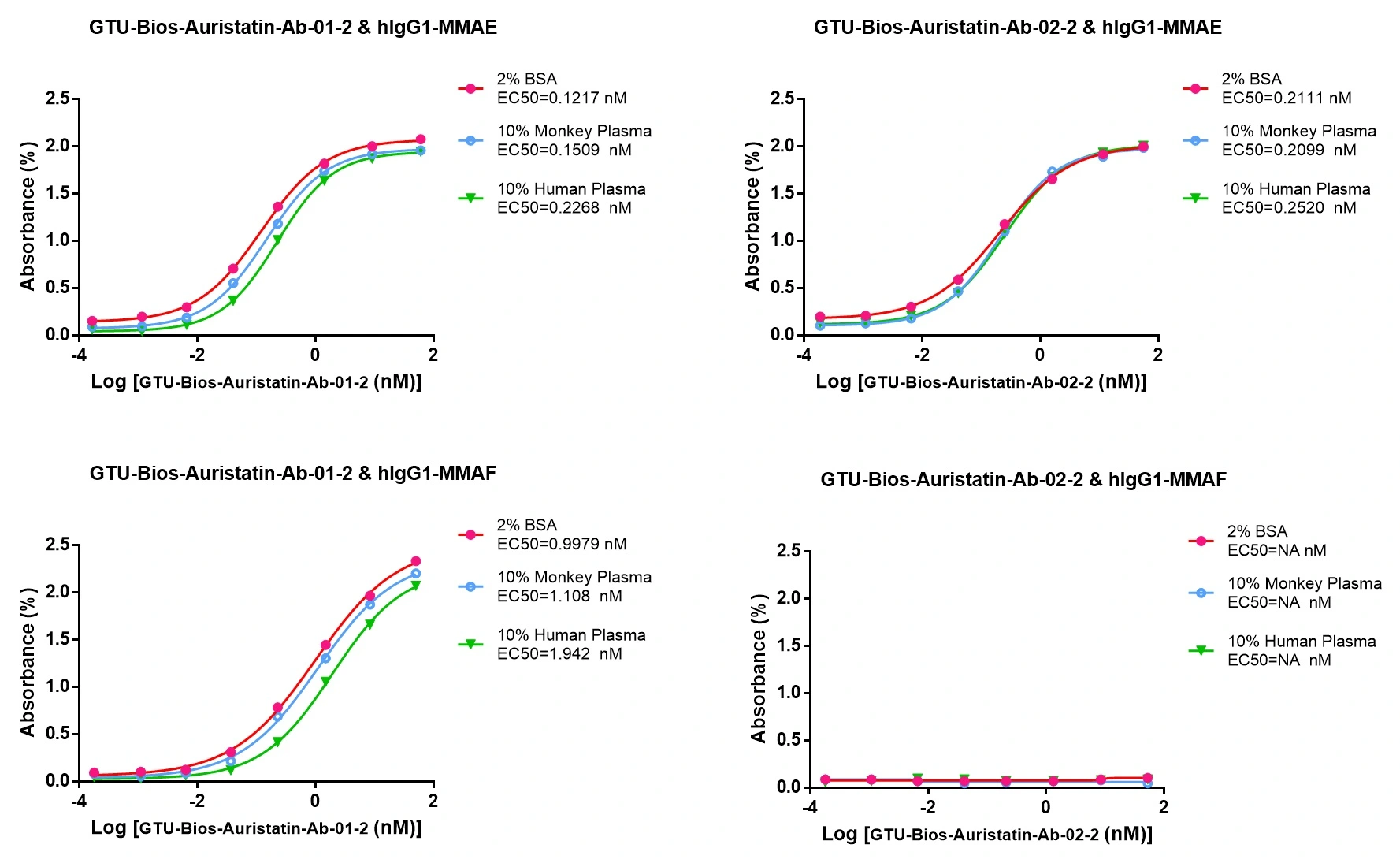
GTU-Bios-Auristatin-Ab-01-2およびGTU-Bios-Auristatin-Ab-02-2はヒトおよびサルを含む薬物動態(PK)研究に使用できます。
GTU-Bios-Auristatin-Ab-01-2はヒトおよびサルのPK研究において最小限の影響を与え、無視できると考えられます。GTU-Bios-Auristatin-Ab-02-2はこれらのPK研究においてGTU-Bios-Auristatin-Ab-01-2よりも影響が少なくなります。GTU-Bios-Auristatin-Ab-01-2およびGTU-Bios-Auristatin-Ab-02-2はヒトおよびサルのPK実験に使用するのに適しています。
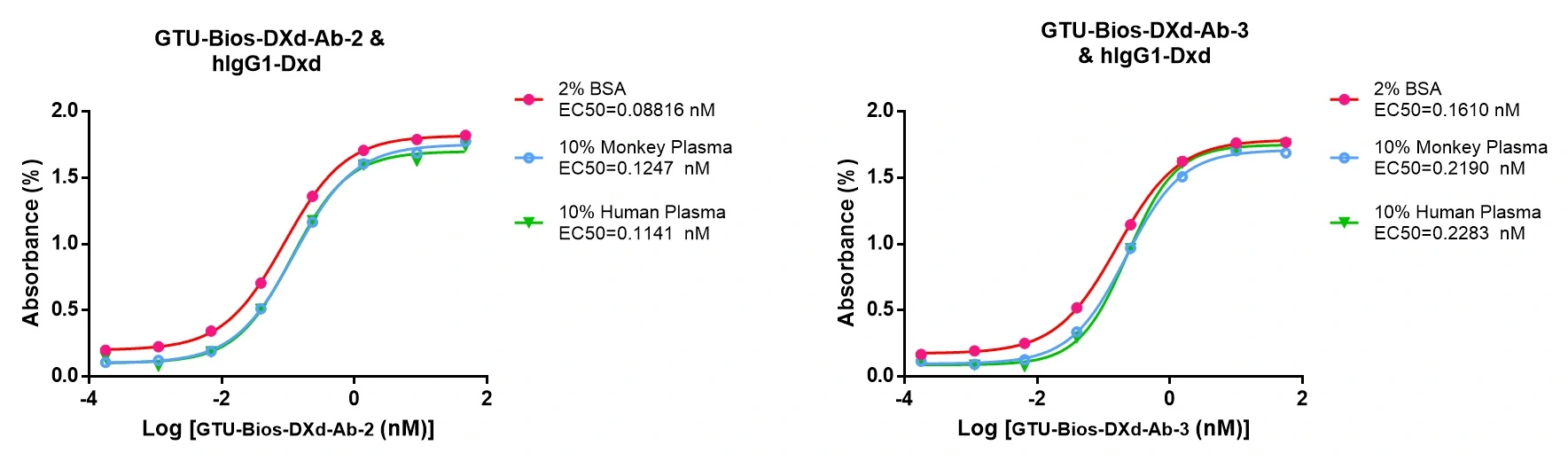
図2. GTU-Bios-DXd-Abはヒトおよびサルの薬物動態(PK)研究において最小限の影響を示します。
GTU-Bios-DXd-AbはヒトおよびサルのPK研究において最小限の影響を示し、これらの実験での適用に適しています。
抗体薬物複合体(ADC、Antibody-Drug Conjugates)の「抗ペイロード抗体」の概念は、ADC治療の開発と最適化においてユニークな戦略を含んでいます。通常、ADCは化学リンカーを介して抗体に結合された細胞毒性薬物(ペイロード)で構成されています。ADCの抗体部分はがん細胞の特定の抗原を標的とし、これらの細胞に細胞毒性ペイロードを直接届け、正常細胞を守りながら殺します。
一方、「抗ペイロード抗体」はペイロード分子を認識して結合するように設計されています。これには複数の目的が含まれます:
安全性と毒性管理:体内で非特異的に放出された自由なペイロード分子に結合することで、これらの抗体はオフターゲット毒性を減少させ、ADC治療の安全性プロファイルを向上させる可能性があります。
精度の向上:ペイロードの生体内分布とクリアランスをよりよく理解するために研究で使用され、より効率的でターゲットに特化したADCの設計に繋がります。
薬物モニタリング:抗ペイロード抗体は、患者のシステム内の薬物レベルを監視するアッセイの開発に役立ち、個別の投与量調整を可能にします。
このアイデアはまだこの分野では新しいですが、抗ペイロード抗体の開発は、がん治療における副作用を最小限に抑えつつ、治療効果を最大化することを目的としたADC技術をさらに精緻化する革新的なアプローチを表しています。

